新闻动态

新捷报,捷闻报 了解最新捷闻咨询
网络直播课 | 聚焦母婴热门产品“吸奶器”:全球市场现状与主流市场合规准入要点分析

2026-01-30
直播主题:
聚焦母婴热门产品“吸奶器”:全球市场现状与主流市场合规准入要点分析
随着母乳喂养需求持续升级,叠加智能化、便携化技术浪潮推动,吸奶器已成为母婴赛道的核心热门产品,企业出海布局意愿强烈,全球市场拓展与合规准入已成为决定企业核心竞争力的关键议题。
鉴于不同国家和地区对吸奶器的产品定义与准入存在显著差异,合规门槛参差不齐。我们将从产品本质出发,拆解吸奶器核心特点与准入差异,分析全球市场规模及销售态势,系统梳理主流市场合规准入要求,逐步带大家全方位掌握行业核心信息,助力企业精准解决吸奶器选品定位、出海合规申报、风险规避等核心痛点,抢占全球市场先机。
课程亮点
一、吸奶器产品核心特点、分类及合规设计核心指引
二、全球吸奶器市场规模及销售现状分析
三、主流出海市场合规准入要求与企业合规风险提示
锁定直播,在线互动,抢占制胜先机!
云课堂时间
2026年02月5日 周四 15:00-16:00(北京时间)
报名链接

扫描上方二维码报名
报名期间有任何疑问欢迎随时联系我们的工作人员!
我们期待您的参与,与您在课程上相聚,共同开启全球医械合规准入的新篇章。
让我们携手共进,把握机遇,迎接挑战!
参与方式与专属福利
回放通道
直播结束后,可通过「Share Info全球医械资讯」公众号观看完整回放,随时复习核心要点;
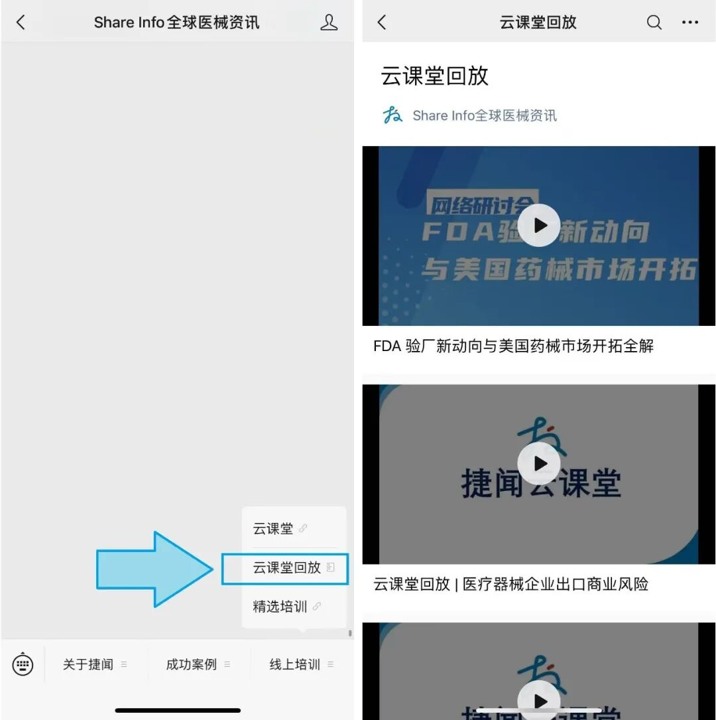
互动升级
联系客服即可加入捷闻专属培训群,获取直播课件、法规原文等独家资料,与行业同行实时交流;同时可进行直播主题推荐,您关心的合规话题我们优先安排!

2026 年,捷闻与您每周四相约免费直播,以专业解读赋能合规实践,助力医械企业从容应对全球监管变革!
End
获取更多相关信息, 您也可以直接联系我们。
我们将竭诚为您服务!



